2. 青岛海洋科学与技术试点国家实验室, 海洋渔业科学与食物产出过程功能实验室, 山东 青岛 266071
2. Laboratory for Marine Fisheries Science and Food Production Processes, Pilot National Laboratory for Marine Sci-ence and Technology(Qingdao), Qingdao 266071, China
长链非编码RNA (long non-coding RNA, lncRNA)是一种长度超过200个碱基且不翻译产生蛋白质的RNA[1]。Xist是最早被发现的lncRNA之一, 它的功能是在雌性哺乳动物中控制两条X染色体中的一条染色体沉默, 从而起到剂量补偿效应的作用[2]。多项研究表明, lncRNA在剂量补偿效应[3]、调控mRNA的表达[4]和降解[5]、构成细胞核内亚结构的结构骨架[6]、作为染色体重塑的调节因子[7]等方面发挥着重要的作用。lncRNA与mRNA皆是由RNA聚合酶Ⅱ转录而后拼接形成的, 部分lncRNA还具有多聚核苷酸的尾巴, 但lncRNA与mRNA的不同之处是其不含编码区并且保守性较低[8]。lncRNA主要分布在生物的细胞核中, 但也有少部分lncRNA分布在细胞质或细胞器中[9]。根据lncRNA与其相邻的编码基因的位置关系, 有研究者将lncRNA分为3类: (1)位于编码基因与编码基因之间的lncRNA, 又称lincRNA (long intergenic noncoding RNA); (2)编码基因内含子区lncRNA; (3)编码基因反义链lncRNA[10]。lncRNA在生物体内的作用机制主要可以分为5种: (1)信号作用, 如在DNA受损后, P53结合到cdkn1a的启动子区域, 激活lncRNA panda, panda进一步作用于NF-YA蛋白质, 从而限制凋亡前体基因的表达, 最终使细胞周期停滞[11]; (2)诱饵作用, 如lncRNA gas5可以竞争性地与糖皮质激素受体DNA结合区域结合, 进而抑制受体和染色体的相互作用[12]; (3)海绵作用, 如lncRNA ptenp1可能吸附某些特定miRNA, 从而调控某些受该miRNA靶基因的表达[13]; 具备该作用的lncRNA也被称为ceRNA (competing endogenous RNA), 即竞争性内源RNA[14]; (4)引导作用, 如植物中的lncRNA coldair可以引导PRC2复合体到达flc基因的染色体位置, 通过H3K27的三甲基化调控基因表达[15]; (5)支架作用, lncRNA hotair可以与PRC2蛋白复合体结合, 同时还可以与另一个包含LSD1、CoREST及REST等蛋白因子的去甲基化蛋白复合体结合, 从而起到连接支架的作用[16]。
多项研究表明, lncRNA参与了生物的有性生殖[17]、性腺发育[18]、减数分裂[19]、配子形成[20-21]等过程。在黑龙江鲟(Acipenser schrenckii)[22]、中华鳖(Pelodiscus sinensis)[23]和小鼠[24]中, 通过生物信息学方法发现了多条lncRNA靶向与生殖相关的基因。Dmrt (double-sex and mab-3 relatated transcription factor)基因家族是指编码具有高度保守的DNA结合结构域的转录因子的一类基因, 该基因家族编码的蛋白可以以锌指方式与特定DNA序列结合并调控下游基因的表达, 从而参与性别决定和分化等有关生理发育的过程[25]。dmrt1是DMRT家族的一个成员, 其在青鳉(Oryzias latipes)[26]和半滑舌鳎(Cynoglossus semilaevis)[27-28]中被鉴定为性别决定基因。在小鼠中, lncRNA Dmr参与Dmrt1转录后的剪接过程[29]。Wen等[30]使用基因敲除技术敲除了果蝇中105个在睾丸中特异表达的lncRNA, 其中的33个lncRNA的缺失会导致雄性果蝇精子发生可见的发育缺陷, 并失去生殖能力。以上研究都表明lncRNA在动物的性别分化与发育、成熟中发挥着重要的作用。
大黄鱼(Larimichthys crocea)是中国重要的海洋经济鱼类之一。大黄鱼在个体大小和生长速率等方面存在显著的雌雄二态性, 雌鱼的生长速度明显快于雄鱼, 性成熟时雌鱼的均重明显比雄鱼高, 因此繁育大黄鱼的全雌群体被认为是提高大黄鱼养殖效率的一种有效方式。虽然本实验室之前就已经建立了通过将人工雌核发育产生的大黄鱼苗诱导性反转培育伪雄鱼(XX♂), 再通过伪雄鱼与雌鱼配组生产遗传全雌大黄鱼的技术[31], 但是仍存在一些问题, 例如伪雄鱼生长发育迟缓, 个体严重偏小, 产精量比较低。为解决上述问题, 需要开发新的大黄鱼性别控制育种技术, 为此对大黄鱼性别决定和性腺发育与分化调控机制开展深入研究十分必要。
本实验室通过构建大黄鱼高密度遗传图谱并结合QTL定位技术, 已将雄性性别决定区间定位到了9号染色体的28~37.1 cM区域[32], 在此区域内发现了68个基因, dmrt1 (doublesex and mab-3 related transcription factor 1)是该区域中在雌雄性腺中差异表达最显著的基因[33]。lncRNA在黑龙江鲟[22]、中华鳖[23]、小鼠[29]、果蝇[30]等生物性腺中的研究表明lncRNA在动物性腺中发挥着重要作用, 由此推测lncRNA在大黄鱼的性腺发育中也可能起着重要作用。因此, 本研究利用生物信息学的方法挖掘大黄鱼性腺中的lncRNA, 以期筛选到与性腺发育和分化相关的lncRNA, 为阐明大黄鱼性别决定与分化的机制提供基础。
1 材料与方法 1.1 材料在福建宁德的大黄鱼养殖基地, 从生长状态良好、体长20~24 cm的2年龄性成熟大黄鱼养殖群体中随机选取雄鱼和雌鱼各3尾。分别剖取部分精巢和卵巢, 用RNA保护液固定后保存于–80℃超低温冰箱。使用RNA试剂盒(TransZol Up Plus RNA Kit, 全式金生物有限公司)对所取性腺提取总RNA, DNase I消化去除可能混有的DNA。检测合格的样品, 用Epicentre Ribo-zeroTM rRNA Removal Kit (Epicentre, USA)去除rRNA后, 构建链特异性转录组文库, 使用Illumina HiSeq4000平台测序(PE150)。
1.2 转录组的比对组装、注释使用FastQC v0.11.7[34]查看测序后的数据质量, 随后用Trimmomatic v0.36[35]对测序数据进行过滤:去除接头, 截去连续4个碱基平均质量值低于20的部分, 舍去长度短于50 bp的reads (参数: ILLUMINACLIP:TruSeq3-PE-2.fa:2:30:10SLIDIN GWINDOW:4:20 MINLEN: 50)。
使用HISAT2 v2.1.0[36]将过滤后的测序数据比对到本实验室利用三代测序技术组装的大黄鱼基因组(未发表)。对得到的SAM文件, 使用samtools v1.4[37]排序并转换为BAM文件。随后使用StringTie v1.3.4d[38]进行拼接、组装。用gffread[39]得到组装后的转录本序列。
选取每个基因最长的转录本, 使用eggnog- mapper v1.0.3[40]的diamond模式将序列比对到egggnog蛋白数据库v4.5.1[41]进行基因功能注释。
1.3 差异表达基因分析上述组装出的转录本, 使用Python脚本prepDE.py得到基因的reads计数矩阵。随后, 使用DESeq2[42]进行基因层面的差异分析。由于大黄鱼卵巢与精巢中的基因表达差异巨大, 因此执行较严格的筛选条件padj < 0.01, log2(fold change)绝对值大于2。选取前300个差异表达基因对两组雌雄样品进行主成分分析(PCA), 鉴别组内样本的重复性以及组间样品的差异水平。
1.4 候选lncRNA的筛选将拼接得到的转录本使用eggnog-mapper的diamond模式比对到eggnog的蛋白数据库, 无法比对到蛋白数据库的转录本用CPC2[43]和CNCI[44]进行编码潜能的分析, 同时用pfam_scan.pl比对Pfam32.0[45]数据库。最后将CPC2、CNCI预测得到的没有编码能力的转录本, 与未比对到Pfam32.0数据库的转录本取交集, 再将其比对到rfam[46]数据库, 去除tRNA、rRNA, 得到最后的候选lncRNA集。
1.5 lncRNA的靶基因预测在基因组序列上, 取所有差异lncRNA上下游50 kb的所有编码基因, 分别计算该lncRNA与此区域中各编码基因的皮尔森相关系数(Pearson correlation coefficient), 若某编码基因与lncRNA的相关系数大于0.8, P < 0.05, 则认为该编码基因是受该lncRNA调控的靶基因。
2 结果与分析 2.1 测序数据6尾大黄鱼卵巢与精巢组织测序共得到282457758条reads, 每个个体的测序量为13.38~15.32 Gb, 平均14.24 Gb。去除接头序列, 截去连续4个碱基平均质量值低于20的部分, 舍去长度少于50 bp的reads。共得到259935783条reads。过滤后每个个体的测序量为12.36~14.07 Gb, 平均12.98 Gb。每个个体的测序量为每4个碱基的平均质量值均大于20。每个个体的测序深度为17.23 X~19.62 X, 平均测序深度为18.10 X。
2.2 基因注释使用HISAT2将过滤后的测序数据比对到本实验室组装的大黄鱼三代参考基因组(未发表), 平均比对率为91.42%(89.78%~93.60%), 平均的唯一比对率为74.14%(70.60%~78.03%), 通过StringTie拼接得到来自31675个基因的66088个转录本。26277个基因可用eggong-mapper比对到蛋白家族数据库, 其中有Gene symbol的共有13928 (43.97%)个。
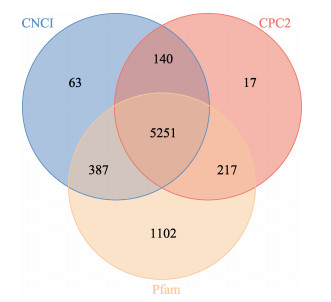
2.3 lncRNA筛选将未能比对到蛋白数据库的转录本, 首先过滤掉长度小于200 bp的转录本。然后, 分别使用CPC2、CNCI和PfamScan 3个软件进行编码能力的预测分析, 得到无编码能力的转录本数目分别是5625、5841和6957条, 将3个软件得到的数据取交集得到5251条lncRNA (图 1)。然后通过比对到rfam数据库去除tRNA和rRNA, 最终共得到来自3984个基因的5162条lncRNA。
|
图 1 CPC2、CNCI、Pfam预测lncRNA的韦恩图 Fig.1 Venn diagram of lncRNAs predicted by CPC2, CNCI and Pfam |
通过DESeq2对数据进行基因层次的处理和统计分析。根据FDR < 0.01以及Fold Change > 2的标准, 共发现卵巢与精巢中差异mRNA有9341个, 其中卵巢相对于精巢表现上调的mRNA有3184个, 下调的mRNA有6157个。在卵巢中特异性表达的mRNA有22个, 在精巢中特异性表达的mRNA有1109个。
根据FDR < 0.01以及Fold Change > 2的标准, 共发现卵巢与精巢中差异lncRNA为2782个, 其中卵巢相对于精巢上调的lncRNA 492个, 下调的lncRNA 2290个。在卵巢中特异性表达的lncRNA有61个, 在精巢中特异性表达的lncRNA有803个。
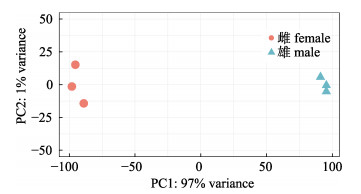
主成分分析显示, 雌雄两组间的差异显著, 而在组内差异性较小。说明组内样本的重复性良好(图 2)。
|
图 2 性腺IncRNA表达量主成分分析 Fig.2 Principle component analysis of gonadal IncRNA expression |
对上述得到的差异表达mRNA进行GO富集分析, 其结果如图 2所示。在biological process (生物学过程)方面, 富集结果最多的有reproduction (繁殖), 富集到了137个差异的mRNA。在cellular component (细胞组成)方面, 富集结果最多的是cytoskeleton (细胞骨架), 富集到了144个差异的mRNA。在molecular function (分子功能)方面, 富集结果最多的是cytoskeletal protein binding (细胞骨架绑定), 富集到了58个差异的mRNA。
在reproduction (繁殖)的GO条目中的基因大多与生物繁殖或细胞分裂相关, 精巢相对于卵巢表达上调的基因有piwil1、cetn1、hormad2等共93个, 卵巢相对于精巢表达上调的基因有bmp15、zp3、nanos3等44个。
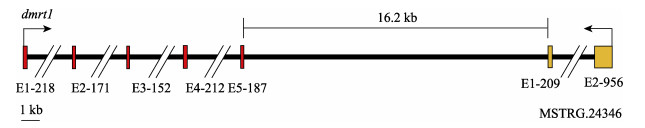
2.6 lncRNA的靶基因分析以距离及表达量的相关性作为筛选条件, 经过计算共得到892个lncRNA与865个mRNA组成的1227对lncRNA-mRNA。其中有44条lncRNA靶向调控了reproduction条目的25个基因, 共组成45对lncRNA-mRNA, 其中包括与精子的发育密切相关的基因piwil1、cetn1、hormad2, 以及与多种动物性别决定密切相关的基因dmrt1 (表 1)。lncRNA MSTRG.24346位于大黄鱼dmrt1基因下游16.2 kb的负链上(图 3), 只在精巢中表达, 而在卵巢中不表达。
|
|
表 1 部分性别相关lncRNA及其靶基因的位置信息、表达量及相关系数 Tab.1 Location, expression and correlation coefficient of partial gender-based lncRNA and its target genes |

|
图 3 差异表达基因的GO富集 Fig.3 Gene ontology (GO) functional annotation of differentially expressed genes |
|
图 4 dmrt1与lncRNA MSTRG.24346位置示意图 方框表示外显子, 外显子编号及长度标注在其下侧, 双斜线表示内含子. Fig.4 The location diagram of dmrt1 and lncRNA MSTRG.24346 Exons are represented by boxes, while the numbers given below it represent the relative base pair sizes of exons. Introns are represented by double slant. |
在其他物种的研究中, 已发现lncRNA与性别分化、性腺发育、配子发生等过程密切相关。在黑龙江鲟精巢与卵巢的lncRNA研究中发现, 多条lncRNA靶向多个与性腺发育和配子发生相关的基因[22]。在中华鳖的精巢与卵巢的lncRNA研究中, 发现多条lncRNA的靶基因中包括dmrt1、sox9、cyp19a、sox3等与性别分化相关的基因[23]。通过基因敲除技术, 证实了某些lncRNA对果蝇的精子发育以及维持生育能力是不可或缺的[30]。
Avasthi等[47]报道, 在雌性小鼠中敲除cetn1后雌性小鼠仍然具有正常生育能力, 但是在雄性小鼠中敲除cetn1基因后, 虽然该小鼠的睾丸大小正常, 精原细胞和精母细胞也发育正常, 但是精子数量却十分稀少, 为数不多的精子大多畸形, 失去了正常生育能力。这说明cetn1基因在雄性小鼠的精子发育晚期发挥着重要作用。Kogo等[48]的研究表明, hormad2是雄性小鼠的精子发生过程中必需的基因, 雄性小鼠敲除hormad2基因后, 其精母细胞凋亡, 睾丸和附睾中检测不到精子的存在, 而敲除雌性小鼠的hormad2基因则不影响其生育能力。Guo等[49]研究发现在无精子症患者中piwi(piwil1)突变, 并通过构建piwi(piwil1)突变的小鼠, 证明了这种突变可以导致雄性小鼠不育, 从而说明piwi(piwil1)的突变是人类不育的一个因素。本研究通过对大黄鱼精巢和卵巢RNA测序数据进行分析, 共挖掘到了3984个lncRNA, 并预测得到了1227对lncRNA-mRNA; 在lncRNA调控的基因中包括cetn1、hormad2、piwil1 3个精子发生和发育所必需的基因, 其中, lncRNA MSTRG.6099、MSTRG.6100靶向cetn1, lncRNA MSTRG.4543、MSTRG.4561靶向hormad2, lncRNA MSTRG.25008靶向piwil1。这些lncRNA与其靶基因的皮尔森相关系数的绝对值都大于0.9, P值均小于0.05。MSTRG.25008与其靶基因piwil1之间呈现负相关, 其余的lncRNA与其靶基因都呈现高度的正相关。说明大黄鱼性腺发育(至少是精子发生和发育)过程可能也受到lncRNA的调控。
除此之外, 本研究还在大黄鱼精巢的转录组中发现一条lncRNA (lncRNA MSTRG.24346), 位于大黄鱼的dmrt1下游16.2 kb的负链上, 表达模式与dmrt1呈极显著的正相关, 皮尔森相关系数达0.992 (P < 0.0001)。本实验室林爱强[33]采用荧光定量PCR技术对大黄鱼dmrt1的时空表达模式进行了研究, 发现dmrt1基因只在雄鱼及伪雄鱼精巢中特异性表达, 在其他组织及雌鱼各组织(包括卵巢)中都检测不到其表达。鉴于dmrt1在多个物种的性别决定起重要作用[26-28], 并且本实验室通过QTL定位找到的性别决定区域中包含有dmrt1, 可以推测dmrt1是大黄鱼的性别决定候选基因。本研究在精巢转录组中发现lncRNA MSTRG.24346的靶基因为dmrt1, 两者之间表达模式完全一致, 说明lncRNA可能在大黄鱼的性别决定中也发挥着一定的作用。
综上所述, 本研究在大黄鱼性腺中挖掘到了3984个基因位点的5162条lncRNA, 2782个lncRNA在精巢与卵巢中差异表达, 高度相关的lncRNA-mRNA对1227, 并在精巢中发现了多条靶向dmrt1、cetn1、hormad2、piwil1等与雄性性别决定和性腺发育相关基因的lncRNA, 说明大黄鱼的性别决定及性腺发育和分化也受到lncRNA的调控。本研究为大黄鱼雌雄性别决定与分化机制研究提供了一个新的研究方向, 为最终研究阐明其分子调控机理提供了重要的基础资料。
| [1] |
Spizzo R, Almeida M I, Colombatti A, et al. Long non-coding RNAs and cancer: A new frontier of translational research?[J]. Oncogene, 2012, 31(43): 4577-4587. DOI:10.1038/onc.2011.621 |
| [2] |
Lee J T. The X as model for RNA's niche in epigenomic regulation[J]. Cold Spring Harbor Perspectives in Biology, 2010, 2(9): a003749. |
| [3] |
Wutz A, Rasmussen T P, Jaenisch R. Chromosomal silencing and localization are mediated by different domains of Xist RNA[J]. Nature Genetics, 2002, 30(2): 167-174. DOI:10.1038/ng820 |
| [4] |
Zhou Z Y, Li A M, Adeola A C, et al. Genome-wide identification of long intergenic noncoding RNA genes and their potential association with domestication in pigs[J]. Genome Biology and Evolution, 2014, 6(6): 1387-1392. DOI:10.1093/gbe/evu113 |
| [5] |
Gong C G, Maquat L E. lncRNAs transactivate STAU1- mediated mRNA decay by duplexing with 3′ UTRs via Alu elements[J]. Nature, 2011, 470(7333): 284-288. DOI:10.1038/nature09701 |
| [6] |
Clemson C M, Hutchinson J N, Sara S A, et al. An architectural role for a nuclear noncoding RNA: NEAT1 RNA is essential for the structure of paraspeckles[J]. Molecular Cell, 2009, 33(6): 717-726. DOI:10.1016/j.molcel.2009.01.026 |
| [7] |
Gupta R A, Shah N, Wang K C, et al. Long non-coding RNA HOTAIR reprograms chromatin state to promote cancer metastasis[J]. Nature, 2010, 464(7291): 1071-1076. DOI:10.1038/nature08975 |
| [8] |
Rinn J L, Chang H Y. Genome regulation by long noncoding RNAs[J]. Annual Review of Biochemistry, 2012, 81: 145-166. DOI:10.1146/annurev-biochem-051410-092902 |
| [9] |
Derrien T, Johnson R, Bussotti G, et al. The GENCODE v7 catalog of human long noncoding RNAs: Analysis of their gene structure, evolution, and expression[J]. Genome Research, 2012, 22(9): 1775-1789. DOI:10.1101/gr.132159.111 |
| [10] |
Moran V A, Perera R J, Khalil A M. Emerging functional and mechanistic paradigms of mammalian long non-coding RNAs[J]. Nucleic Acids Research, 2012, 40(14): 6391-6400. DOI:10.1093/nar/gks296 |
| [11] |
Hung T, Wang Y L, Lin M F, et al. Extensive and coordinated transcription of noncoding RNAs within cell-cycle promoters[J]. Nature Genetics, 2011, 43(7): 621-629. DOI:10.1038/ng.848 |
| [12] |
Kino T, Hurt D E, Ichijo T, et al. Noncoding RNA Gas5 is a growth arrest- and starvation-associated repressor of the glucocorticoid receptor[J]. Science Signaling, 2010, 3(107): ra8. |
| [13] |
Poliseno L, Salmena L, Zhang J W, et al. A coding-independent function of gene and pseudogene mRNAs regulates tumour biology[J]. Nature, 2010, 465(7301): 1033-1038. DOI:10.1038/nature09144 |
| [14] |
Salmena L, Poliseno L, Tay Y, et al. A ceRNA hypothesis: The Rosetta Stone of a hidden RNA language?[J]. Cell, 2011, 146(3): 353-358. DOI:10.1016/j.cell.2011.07.014 |
| [15] |
Heo J B, Sung S. Vernalization-mediated epigenetic silencing by a long intronic noncoding RNA[J]. Science, 2011, 331(6013): 76-79. DOI:10.1126/science.1197349 |
| [16] |
Tsai M C, Manor O, Wan Y, et al. Long noncoding RNA as modular scaffold of histone modification complexes[J]. Science, 2010, 329(5992): 689-693. DOI:10.1126/science.1192002 |
| [17] |
Zhang Y C, Liao J Y, Li Z Y, et al. Genome-wide screening and functional analysis identify a large number of long noncoding RNAs involved in the sexual reproduction of rice[J]. Genome Biology, 2014, 15(12): 512. DOI:10.1186/s13059-014-0512-1 |
| [18] |
Taylor D H, Chu E T, Spektor R, et al. Long non-coding RNA regulation of reproduction and development[J]. Molecular Reproduction and Development, 2015, 82(12): 932-956. DOI:10.1002/mrd.22581 |
| [19] |
van Werven F J, Neuert G, Hendrick N, et al. Transcription of two long noncoding RNAs mediates mating-type control of gametogenesis in budding yeast[J]. Cell, 2012, 150(6): 1170-1181. DOI:10.1016/j.cell.2012.06.049 |
| [20] |
Herrera L, Ottolenghi C, Garcia-Ortiz J E, et al. Mouse ovary developmental RNA and protein markers from gene expression profiling[J]. Developmental Biology, 2005, 279(2): 271-290. DOI:10.1016/j.ydbio.2004.11.029 |
| [21] |
Laiho A, Kotaja N, Gyenesei A, et al. Transcriptome profiling of the murine testis during the first wave of spermatogenesis[J]. PLoS ONE, 2013, 8(4): e61558. DOI:10.1371/journal.pone.0061558 |
| [22] |
Zhang X, Shi J L, Sun Y L, et al. Transcriptome analysis provides insights into differentially expressed genes and long noncoding RNAs involved in sex-related differences in Amur sturgeon (Acipenser schrenckii)[J]. Molecular Reproduction and Development, 2019, 86(2): 132-144. DOI:10.1002/mrd.23065 |
| [23] |
Zhang J, Yu P, Zhou Q Y, et al. Screening and characterisation of sex differentiation-related long non-coding RNAs in Chinese soft-shell turtle (Pelodiscus sinensis)[J]. Scientific Reports, 2018, 8: 8630. DOI:10.1038/s41598-018-26841-3 |
| [24] |
Sun J, Lin Y, Wu J. Long non-coding RNA expression profiling of mouse testis during postnatal development[J]. PLoS ONE, 2013, 8(10): e75750. DOI:10.1371/journal.pone.0075750 |
| [25] |
Raymond C S, Shamu C E, Shen M M, et al. Evidence for evolutionary conservation of sex-determining genes[J]. Nature, 1998, 391(6668): 691-695. DOI:10.1038/35618 |
| [26] |
Matsuda M, Nagahama Y, Shinomiya A, et al. DMY is a Y-specific DM-domain gene required for male development in the medaka fish[J]. Nature, 2002, 417(6888): 559-563. DOI:10.1038/nature751 |
| [27] |
Chen S L, Zhang G J, Shao C W, et al. Whole-genome sequence of a flatfish provides insights into ZW sex chromosome evolution and adaptation to a benthic lifestyle[J]. Nature Genetics, 2014, 46(3): 253-260. DOI:10.1038/ng.2890 |
| [28] |
Cui Z K, Liu Y, Wang W W, et al. Genome editing reveals dmrt1 as an essential male sex-determining gene in Chinese tongue sole (Cynoglossus semilaevis)[J]. Scientific Reports, 2017, 7: 42213. DOI:10.1038/srep42213 |
| [29] |
Zhang L, Lu H, Xin D Z, et al. A novel ncRNA gene from mouse chromosome 5 trans-splices with Dmrt1 on chromosome 19[J]. Biochemical and Biophysical Research Communications, 2010, 400(4): 696-700. DOI:10.1016/j.bbrc.2010.08.130 |
| [30] |
Wen K J, Yang L J, Xiong T L, et al. Critical roles of long noncoding RNAs in Drosophila spermatogenesis[J]. Genome Research, 2016, 26(9): 1233-1244. DOI:10.1101/gr.199547.115 |
| [31] |
Wang Z Y, Cai M Y, Xie Y J. Female nuclear development and sex control techniques in large yellow croaker[M]// Chen S L. Fish Sex Control and Cell Engineering Breeding. Beijing: Science Press, 2013: 274-296. [王志勇, 蔡明夷, 谢仰杰.大黄鱼雌核发育和性别控制技术[M]//陈松林.鱼类性别控制与细胞工程育种.北京: 科学出版社, 2013: 274-296]
|
| [32] |
Wang Z Y, Cai M Y. Artificial gynogenesis and sex control in large yellow croaker[M]//Wang H P, Piferrer F, Chen S L, et al. Sex Control in Aquaculture. Hoboken: John Wiley & Sons, 2018: 751-773.
|
| [33] |
Lin A Q. Study of sex-specific molecular markers and some sexrelated genes in large yellow croaker (Larimichthys crocea)[D]. Xiamen: Jimei University, 2017. [林爱强.大黄鱼性别特异分子标记及部分性别相关基因的初步研究[D].厦门: 集美大学, 2017.]
|
| [34] |
Andrews S. Fast QC: A quality control tool for high throughput sequence data[CP/OL]. https://www.bioinformatics.babraham.ac.uk/projects/fastqc/.
|
| [35] |
Bolger A M, Lohse M, Usadel B. Trimmomatic: A flexible trimmer for Illumina sequence data[J]. Bioinformatics, 2014, 30(15): 2114-2120. DOI:10.1093/bioinformatics/btu170 |
| [36] |
Kim D, Langmead B, Salzberg S L. HISAT: A fast spliced aligner with low memory requirements[J]. Nature Methods, 2015, 12(4): 357-360. DOI:10.1038/nmeth.3317 |
| [37] |
Li H, Handsaker B, Wysoker A, et al. The sequence alignment/map format and SAMtools[J]. Bioinformatics, 2009, 25(16): 2078-2079. DOI:10.1093/bioinformatics/btp352 |
| [38] |
Pertea M, Pertea G M, Antonescu C M, et al. StringTie enables improved reconstruction of a transcriptome from RNA-seq reads[J]. Nature Biotechnology, 2015, 33(3): 290-295. DOI:10.1038/nbt.3122 |
| [39] |
Trapnell C, Roberts A, Goff L, et al. Differential gene and transcript expression analysis of RNA-seq experiments with TopHat and Cufflinks[J]. Nature Protocols, 2012, 7(3): 562-578. DOI:10.1038/nprot.2012.016 |
| [40] |
Huerta-Cepas J, Forslund K, Coelho L P, et al. Fast genome-wide functional annotation through orthology assignment by eggNOG-Mapper[J]. Molecular Biology and Evolution, 2017, 34(8): 2115-2122. DOI:10.1093/molbev/msx148 |
| [41] |
Huerta-Cepas J, Szklarczyk D, Forslund K, et al. eggNOG 4.5: A hierarchical orthology framework with improved functional annotations for eukaryotic, prokaryotic and viral sequences[J]. Nucleic Acids Research, 2016, 44(D1): D286-D293. DOI:10.1093/nar/gkv1248 |
| [42] |
Love M I, Huber W, Anders S. Moderated estimation of fold change and dispersion for RNA-seq data with DESeq2[J]. Genome Biology, 2014, 15(12): 550. DOI:10.1186/s13059-014-0550-8 |
| [43] |
Kang Y J, Yang D C, Kong L, et al. CPC2: a fast and accurate coding potential calculator based on sequence intrinsic features[J]. Nucleic Acids Research, 2017, 45(W1): W12-W16. DOI:10.1093/nar/gkx428 |
| [44] |
Sun L, Luo H T, Bu D C, et al. Utilizing sequence intrinsic composition to classify protein-coding and long non-coding transcripts[J]. Nucleic Acids Research, 2013, 41(17): e166. DOI:10.1093/nar/gkt646 |
| [45] |
El-Gebali S, Mistry J, Bateman A, et al. The Pfam protein families database in 2019[J]. Nucleic Acids Research, 2019, 47(D1): D427-D432. DOI:10.1093/nar/gky995 |
| [46] |
Kalvari I, Argasinska J, Quinones-Olvera N, et al. Rfam 13.0: Shifting to a genome-centric resource for non-coding RNA families[J]. Nucleic Acids Research, 2018, 46(D1): D335-D342. DOI:10.1093/nar/gkx1038 |
| [47] |
Avasthi P, Scheel J F, Ying G, et al. Germline deletion of Cetn1 causes infertility in male mice[J]. Journal of Cell Science, 2013, 126(14): 3204-3213. DOI:10.1242/jcs.128587 |
| [48] |
Kogo H, Tsutsumi M, Inagaki H, et al. HORMAD2 is essential for synapsis surveillance during meiotic prophase via the recruitment of ATR activity[J]. Genes to Cells, 2012, 17(11): 897-912. DOI:10.1111/gtc.12005 |
| [49] |
Gou L T, Kang J Y, Dai P, et al. Ubiquitination-deficient mutations in human Piwi cause male infertility by impairing histone-to-protamine exchange during spermiogenesis[J]. Cell, 2017, 169(6): 1090-1104. DOI:10.1016/j.cell.2017.04.034 |
 2019, Vol. 26
2019, Vol. 26

